Carbonate de Calcium - Omya Violette
Le carbonate de calcium (CaCO₃) est un composé chimique naturel présent dans le calcaire, la craie et le marbre, utilisé en tant que charge minérale, correcteur de pH et composant du ciment et des peintures.
Expédition
Dans toute l'Europe
Paiement sécurisé
CB, Virement, Paypal ...
Aussi appelé Blanc de Meudon, de Troyes ou d’Espagne, le Carbonate de Calcium est une très fine craie 100% naturelle utilisée pour de nombreuses applications. Ce composé chimique inorganique naturellement présent dans les roches calcaires, le marbre, la craie et les coquilles d’organismes marins. Il constitue l’un des minéraux les plus abondants sur Terre et joue un rôle essentiel dans de nombreux domaines industriels et biologiques.
Sur le plan physique, le carbonate de calcium se présente sous la forme d’une poudre blanche, insoluble dans l’eau pure mais soluble dans les solutions acides. Il possède une densité d’environ 2,7 g/cm³ et une température de décomposition avoisinant les 825°C, où il libère du dioxyde de carbone pour former de l’oxyde de calcium (chaux vive).
L’histoire de l’utilisation du Carbonate de Calcium remonte à l’Antiquité, où il servait dans la construction, notamment pour la fabrication de mortiers à base de chaux. Aujourd’hui, il est largement employé dans l’industrie des matériaux de construction, la fabrication de peintures, de plastiques, de papiers et dans l’agriculture comme amendement calcaire.
Son procédé de fabrication industrielle repose sur l’extraction de roches calcaires, suivie de leur broyage et purification. Pour obtenir du carbonate de calcium précipité (PCC), on dissout la chaux vive dans l’eau pour produire de l’hydroxyde de calcium, qui réagit ensuite avec du dioxyde de carbone pour précipiter sous forme pure.
Chimiquement, le carbonate de calcium réagit avec les acides pour libérer du dioxyde de carbone. Il intervient également dans la régulation du pH des sols et dans les cycles géochimiques du carbone.
Grâce à ses nombreuses applications et à son abondance naturelle, le Carbonate de Calcium demeure un matériau clé dans de nombreux secteurs industriels et environnementaux.
PRINCIPALES UTILISATIONS
Le carbonate de calcium (CaCO₃) possède de nombreuses utilisations dans divers secteurs industriels, agricoles et médicaux. Voici ses principales applications :
1. Industrie des matériaux de construction
- Fabrication du ciment et du béton
- Production de chaux vive (CaO) et de chaux éteinte (Ca(OH)₂)
- Ingrédient dans le mortier et les enduits
2. Industrie du papier et du plastique
- Charge minérale pour améliorer la blancheur et la résistance du papier
- Agent de charge dans les plastiques (PVC, polypropylène) pour renforcer leur rigidité
3. Agriculture
- Amendement calcaire pour corriger l’acidité des sols et améliorer la croissance des plantes
- Complément alimentaire pour le bétail, apportant du calcium essentiel
4. Traitement des eaux et protection de l’environnement
- Neutralisation des eaux acides dans les stations d’épuration
- Réduction des émissions de soufre dans les centrales thermiques (désulfuration des gaz)
5. Industrie chimique
- Source de dioxyde de carbone (CO₂) par décomposition thermique
- Production de bicarbonate de sodium (NaHCO₃)
6. Autres applications
- Composant de la craie scolaire et des peintures
- Fabrication de verre et de céramiques
Grâce à sa disponibilité et à son faible coût, le carbonate de calcium est un matériau clé dans de nombreux domaines industriels et environnementaux.
CARACTÉRISTIQUES
- Formule brute : CaCO3
- Origine : France
- Pureté : 98%
- Numéro Cas : 1317-65-3
- Numéro CE : 215-279-6
- Numéro UN : non réglementé
- Qualité : technique
Le Carbonate de Calcium naturel est de grande pureté chimique, fin, élaboré à partir d'une craie de Champagne sélectionnée. Omya Etiquette Violette est un polyvalent au rapport performance-coût optimal. Il apporte la rhéologie demandée aux mastics de vitriers.
SYNONYMES (LISTE NON EXHAUSTIVE)
Calcaire, blanc de Meudon, blanc de Troyes, blanc d'Espagne, pierre à chaux, marbre, craie, calcite, aragonite, castine, limestone...
CONSEILS D'EMPLOI
Fabrication de mastic à vitres
- Verser de l'huile de lin sur le Carbonate de Calcium, pétrir jusqu'à obtention d'un Mastic d'une bonne tenue.
Réparation des plaques de marbre cassées
- Préparer un mélange épais de Carbonate de Calcium avec du silicate de soude.
Apport de calcium pour fortifier les pelouses
- En lait que l'on étend à raison de 5kg par 25m².
| Pictogramme(s) | Aucun |
| Phrase(s) de Risque | Aucune |
| Conseil(s) de Sécurité | Aucun |
| Pays de fabrication | France |
|---|---|
| Numéro CE | 215-279-6 |
| Numéro Cas | 1317-65-3 |
| Code Douanier | 28365000 |
Chimiques
| Caractéristiques | Spécifications |
| CaCO3 | 98% |
| MgCO3 | 0.4% |
| Fe2O3 | 0.1% |
| Insolubles HCI | 1% |
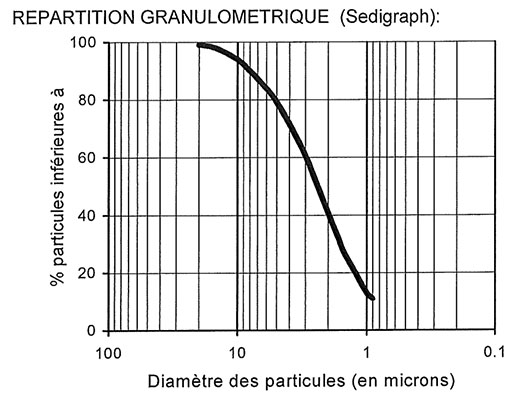
Granulométrique
| Caractéristiques | Spécifications |
| Refus à 45µm (ISO 787/7) | 0.15% |
| Coupe granulométrique (d98%) | 20µm |
| Diamètre moyen des particules (d50%) | 2.4µm |
| Particules < 2µm | 42% |
Physiques
| Caractéristiques | Spécifications |
| Etat physique | Poudre de couleur blanche |
| Odeur | Légère odeur terreuse |
| Densité apparente tassée (ISO 787/11) | 1.1 g / ml |
| Poids moléculaire | 100.08 |
| pH pour une solution saturée de CaCO3 (ISO 787/9) | 9 à 25°C |
| Prise d'huile (ISO 787/5) | 17 g / 100g |
| Prise de DOP (ISO 787/5) | 24 g / 100g |
| Blancheur CIE L*, a*, b* (DIN 6174) | 94 / 0.6 / 4.1 |
| Solubilité dans l'eau | 13 à 16 mg / l à 20°C |
| Taux d'humidité départ usine (ISO 787/2) | 0.2% |
| Point de fusion | Décomposition au dessus de 600°C |
| Point d'ébullition | Décomposition au dessus de 600°C |
| Inflammabilité | Non applicable |